
化粧品GQP・GVP手順書の作成方法|製造販売業許可取得後に整備すべき品質管理体制
※本記事は執筆当時の情報に基づきます。法改正等により現在の内容と異なる場合がありますので、実際の運用にあたっては必ず最新の法令をご確認ください。
化粧品製造販売業の許可を取得したあと、「GQP・GVP手順書をどう作ればいいかわからない」という声をよく聞きます。許可証は交付されたのに、手順書の整備が追いつかないまま販売を開始してしまうケースも珍しくありません。
GQP省令(品質管理基準)とGVP省令(製造販売後安全管理基準)の遵守は、化粧品製造販売業の許可要件です(薬機法第12条の2)。許可取得後も継続して遵守しなければ許可を維持できません。元化学メーカー研究員として化粧品材料の研究開発に携わった経験から、手順書に盛り込むべき実務のポイントを解説します。
GQP・GVPとは
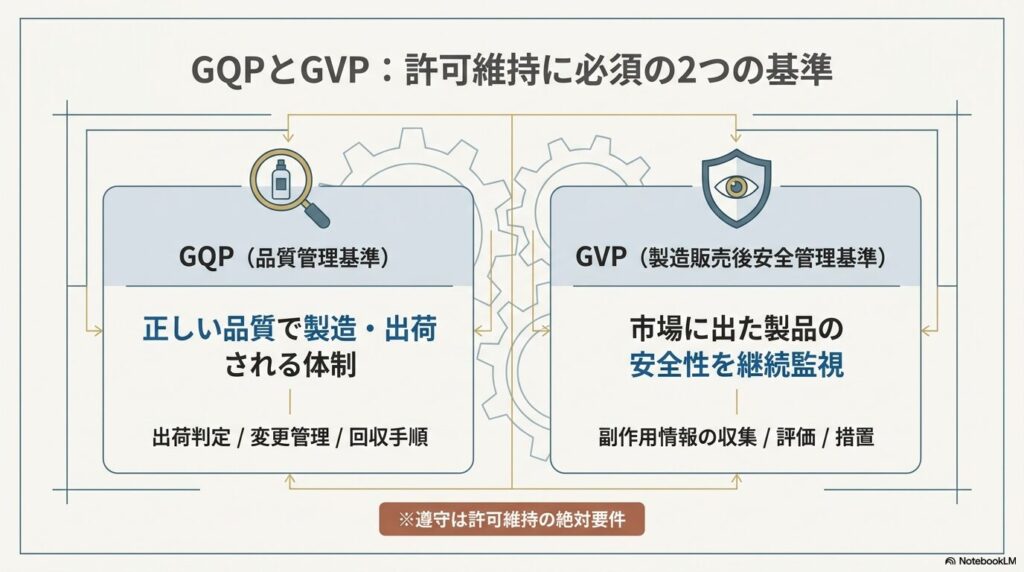
化粧品製造販売業者には、製品の品質管理と安全管理の両面で責任を持つことが求められます。それぞれを規定するのがGQP省令とGVP省令です。
GQP(Good Quality Practice):品質管理基準
製品が正しい品質で製造・出荷されるための管理体制を定めます。出荷判定・変更管理・品質情報の処理・回収手順などが含まれます(平成16年厚生労働省令第136号)。
GVP(Good Vigilance Practice):製造販売後安全管理基準
市場に出回った製品の安全性を継続して監視・管理する体制を定めます。副作用情報の収集・評価・措置立案などが含まれます(平成16年厚生労働省令第135号)。
化粧品の場合、GVP手順書の作成は許可要件として必須ではありませんが、業務の適正を維持するために整備が強く推奨されています。
責任者体制の整備
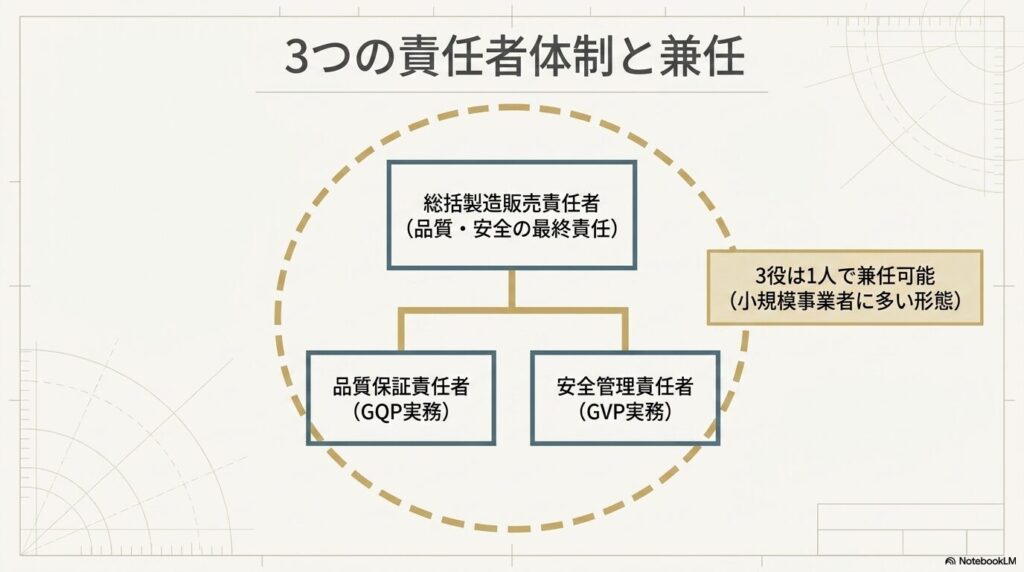
GQP・GVP業務を適正に実施するために、3種類の責任者を設置します(薬機法第17条)。
総括製造販売責任者:品質管理・安全管理の最終責任者。製造管理・品質管理・安全管理に関する業務全体を統括します。薬剤師、または薬学・化学の専門課程修了者等の要件があります(薬機法施行規則第85条の2第2項)。
品質保証責任者:GQP業務の実務責任者。品質保証に関する業務に3年以上従事した経験が必要です。
安全管理責任者:GVP業務の実務責任者。製造販売後安全管理に関する業務を担います。
化粧品製造販売業では、3役を1人が兼任することが可能です。小規模な事業者では、代表者が総括製造販売責任者を兼任しながら、品質保証責任者・安全管理責任者も兼務するケースが多くあります。
GQP手順書の必須項目
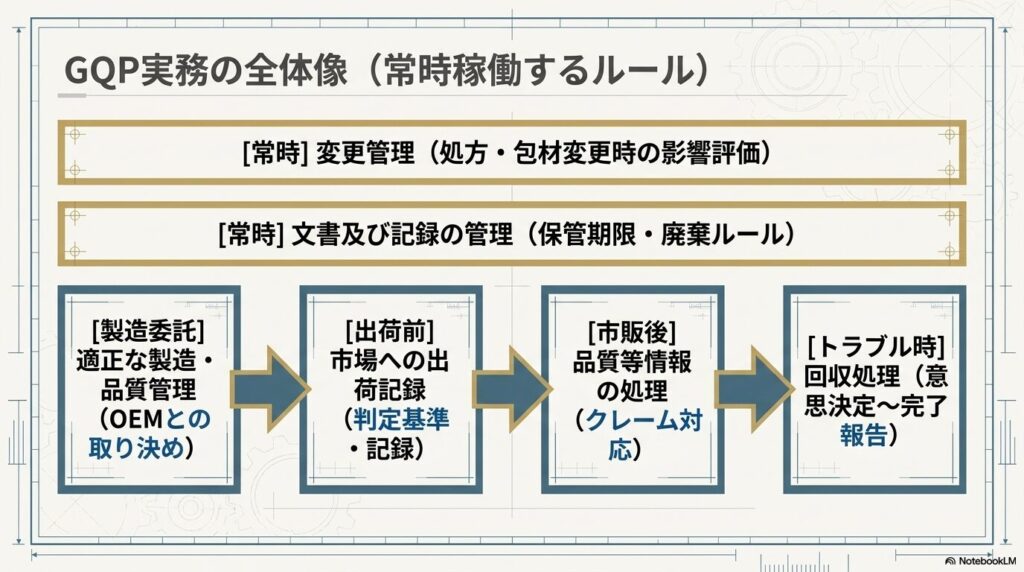
手順書は「作って棚に入れておくもの」ではなく、「常時参照し、その内容に則って業務を行うもの」です(大阪府薬務課)。
GQP業務で整備が必要な主な手順書は次のとおりです。
市場への出荷に係る記録の作成
ロットごとの出荷判定基準・記録様式・保管期限を定めます。適切な検査記録なしに製品を出荷してはなりません。
適正な製造管理及び品質管理の確保
委託製造業者(OEM工場)との取り決め内容を文書化します。OEM委託時は、委託先の製造所が化粧品製造業の許可を持つことを確認した上で、品質に関する取り決め書面を締結します。
変更管理
処方変更・製造所の変更・包材変更など、製品に関する変更が生じた際の手順を定めます。変更の際には品質への影響評価が必要です。
品質等に関する情報及び品質不良等の処理
消費者クレーム・原材料の品質問題・製造トラブルなどの情報を収集・評価し、必要な対応をとる手順です。
回収処理
品質上の問題が発覚した際の回収手順です。回収の意思決定から実施・完了報告までの流れを定めます。
文書及び記録の管理
手順書・記録の作成・保管・廃棄ルールを定めます。記録の保管期限(製品の使用期限後1年間等)も明記します。
GVP手順書の項目
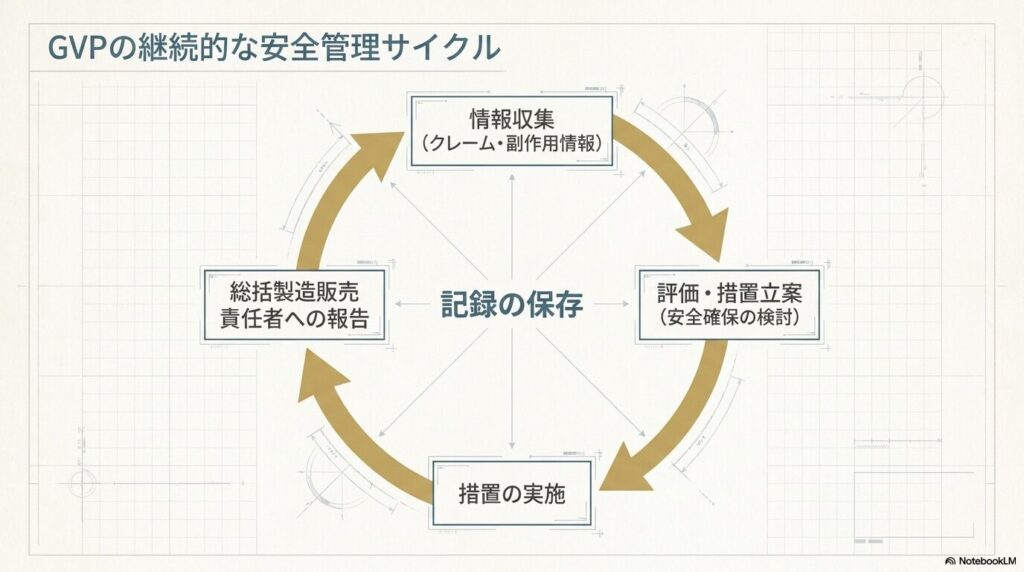
化粧品のGVP手順書で整備を推奨する主な項目です。
- 安全管理情報(クレーム・副作用情報等)の収集方法
- 収集した情報の評価・安全確保措置の立案手順
- 安全確保措置の実施手順
- 総括製造販売責任者への報告ルール
- 記録の保存方法
手順書作成の落とし穴
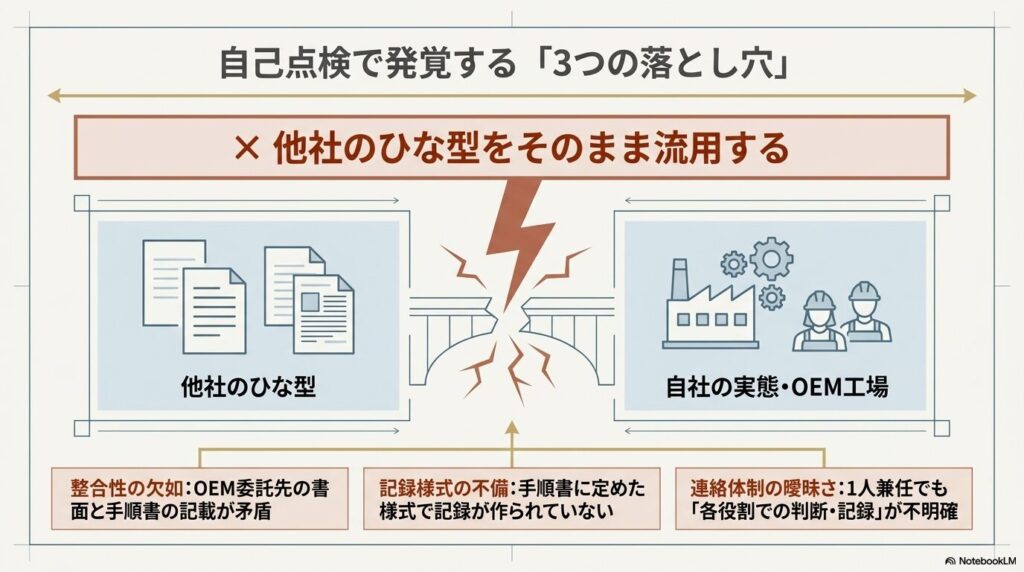
手順書は「自社の業務実態に合わせて作成すること」が重要です。他社のひな型をそのまま流用すると、実際の業務と手順書の内容が乖離し、自己点検(内部監査)の際に問題が発覚します。
特に注意が必要なのは以下の点です。
取り決め内容と手順書の整合性:OEM委託先との書面内容と、GQP手順書の記載が矛盾しないよう確認が必要です。
記録様式の設計:手順書に定めた様式で記録が作成されているか、定期的に確認します。
責任者の連絡体制:3役が1人の場合でも、それぞれの役割で行うべき判断・記録を明確にしておく必要があります。
許可取得後の届出・変更対応
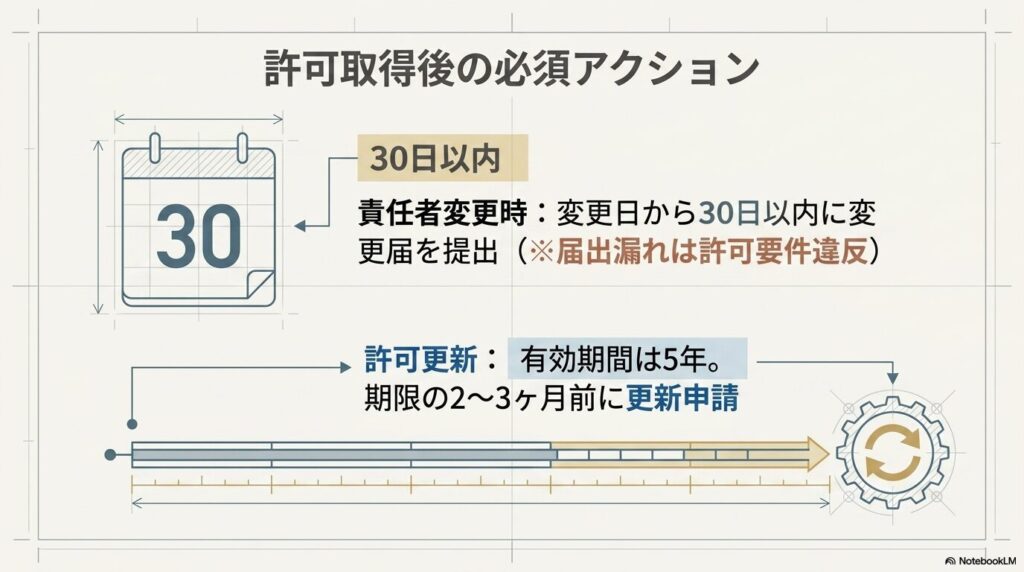
責任者が変更になった場合は、変更の日から30日以内に都道府県知事への変更届が必要です(薬機法第19条第1項・施行規則第99条)。届出を忘れると許可要件の違反状態になるため、人事異動の際に見落とさないよう注意が必要です。
化粧品製造販売業・製造業の許可の有効期間は5年です。更新申請は期限の2〜3ヶ月前(標準事務処理期間60日)に行います。

よくある質問

Q. OEM委託で製造する場合、手順書は誰が作ればいいですか?
A. 製造販売業者(市場への出荷責任を持つ事業者)がGQP・GVP手順書を作成します。製造業者(OEM工場)は別途製造業許可の下で管理を行います。製造販売業者はOEM委託先を監督する立場であり、委託先の品質管理状況を確認する義務があります。
Q. 手順書はどのくらいの頻度で見直せばいいですか?
A. 業務実態に変化が生じたとき(処方変更・製造所変更・責任者変更等)は随時改訂が必要です。変化がない場合でも、年1回の自己点検(内部監査)の中で手順書の内容が実務と整合しているかを確認することを推奨します。
Q. 化粧品製造販売業の許可申請と手順書整備は同時に進めるべきですか?
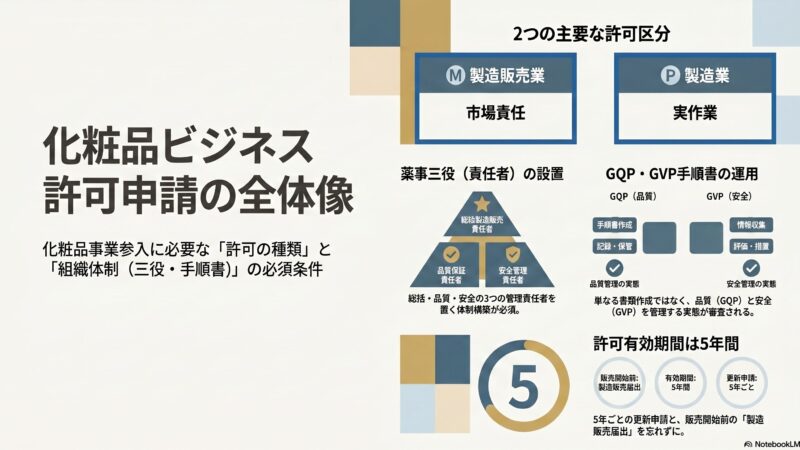
A. 許可申請時には「品質管理・安全管理の方法が省令の基準に適合していること」を示す必要があります。申請段階から手順書の骨格を作成し、許可取得後に詳細化するのが効率的です。化粧品製造販売業許可の全体像も参照してください。
当事務所の強み:化学の専門知識を活かした品質管理体制整備
化粧品の品質管理は、処方・原料・製造プロセスへの理解が不可欠です。元化学メーカー研究員として有機合成・スケールアップ・化粧品材料の研究開発に携わった経験から、処方や製造プロセスを踏まえた実務に即した書類整備を支援します。
- GQP・GVP手順書の作成支援
- 製造委託先との取り決め書面の作成
- 製品ごとの製造販売届出書の作成
- 責任者変更・許可更新手続き
手順書の雛形がない状態でも対応できます。現状の確認からご連絡ください。

