
化粧品許可の更新・変更届|手続き漏れが招く許可失効リスク
※本記事は執筆当時の情報に基づきます。法改正等により現在の内容と異なる場合がありますので、実際の運用にあたっては必ず最新の法令をご確認ください。
化粧品製造販売業・製造業の許可には有効期間があります。更新を怠ると許可が失効し、製造・販売を継続すれば薬機法違反として行政処分等の対象となり得ます。
変更届の漏れも同様です。責任者の交代や事務所の移転が生じた場合に届出を怠ると、許可要件の違反状態が続くことになります。取引先や消費者からの信頼を失うリスクは、製品の品質問題だけではありません。
元化学メーカー研究員として化粧品材料の研究開発に携わった経験から、許可取得後に見落とされやすい維持管理の手続きを整理します。
許可の有効期間と更新タイミング
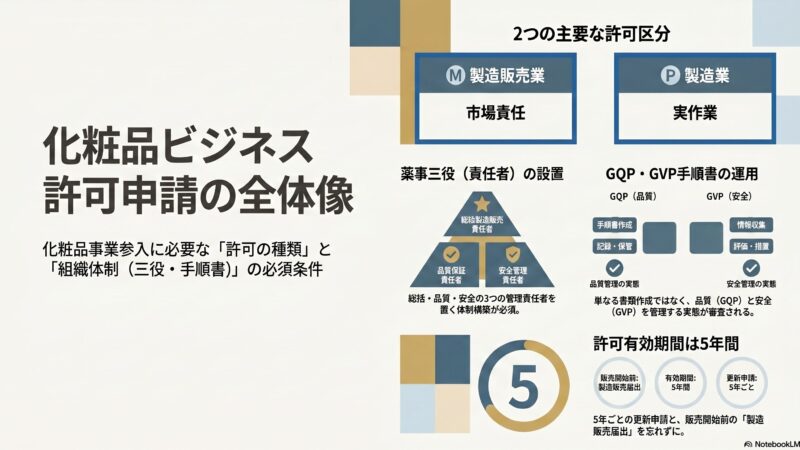
化粧品製造販売業・製造業の許可は、どちらも有効期間が5年間です(薬機法第12条第4項・第13条第4項、施行令第3条・第10条)。許可証に記載された期限日を必ず確認してください。
更新申請は2〜3ヶ月前が必須
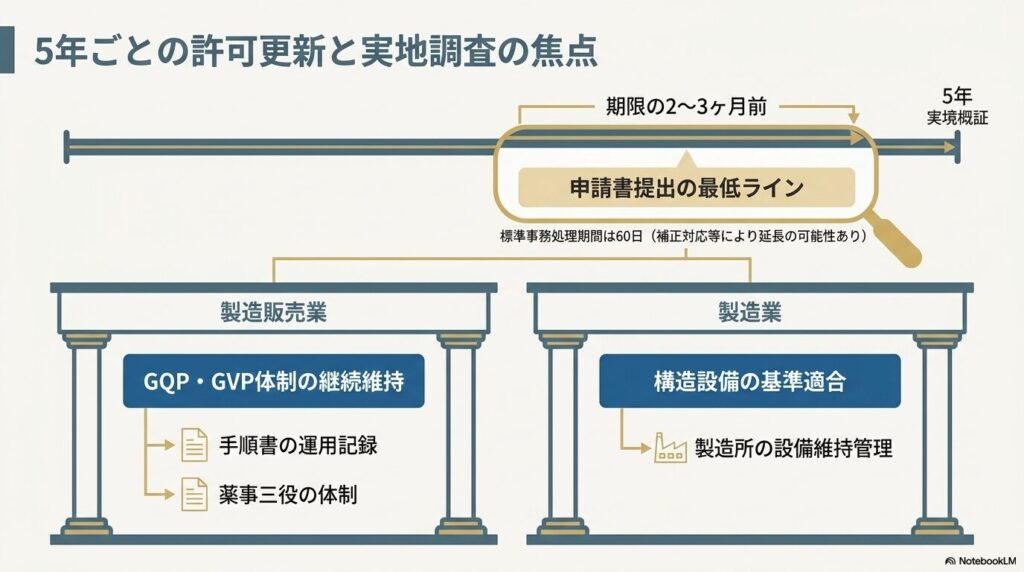
更新申請の標準事務処理期間は60日です(大阪府薬務課、令和6年3月版)。書類の不備があれば補正対応が加わり、さらに時間がかかります。期限の2〜3ヶ月前には申請書を提出するのが最低ラインです。
「まだ2ヶ月ある」と考えていても、書類の準備・薬務課への事前相談・修正対応を経るうちに期限が近づきます。特に責任者の資格証明書類(卒業証明書・在籍証明書等)は取得に時間がかかる場合があります。余裕を持ったスケジュール管理を推奨します。
更新時の実地調査で確認されること
更新申請では、新規取得時と同様に実地調査が行われます。許可の種類によって確認の重点が異なります。
製造販売業の場合:GQP・GVP省令の遵守は許可後も継続して求められる要件です(薬機法第12条の2)。以下の事項が確認対象となります。
- GQP(品質管理)・GVP(安全管理)手順書の整備状況
- 手順書に沿った運用記録(出荷判定記録・クレーム処理記録等)の有無
- 薬事三役(総括製造販売責任者・品質保証責任者・安全管理責任者)の体制維持

製造業の場合:製造所の構造設備が引き続き基準に適合しているかどうかが確認対象となります。
いずれの場合も、許可取得後に管理体制が形骸化していると更新時に手戻りが発生します。日頃の記録管理と設備維持が更新審査の通過を左右します。
変更届が必要なケース
許可内容に変更が生じた場合は、変更の日から30日以内に都道府県知事への変更届が必要です(薬機法第19条第1項・第2項、規則第99条・第100条)。
変更届が必要な主な事項は以下のとおりです。
| 変更事項 | 製造販売業 | 製造業 |
|---|---|---|
| 氏名・住所の変更(法人名・代表者名等) | 変更届 | 変更届 |
| 主たる機能を有する事務所の所在地の変更(大阪府内移転) | 変更届 | 新規申請 |
| 主たる機能を有する事務所の所在地の変更(他都道府県への移転) | 新規申請 | 新規申請 |
| 法人役員(薬事責任役員)の変更 | 変更届 | 変更届 |
| 総括製造販売責任者・責任技術者の変更 | 変更届 | 変更届 |
| 製造所の構造設備の主要部分の変更 | ― | 変更届 |
| 事業(製造所)の廃止 | 廃止届 | 廃止届 |
(出典:大阪府健康医療部生活衛生室薬務課、R6.3版)
製造販売業の「主たる機能を有する事務所」は品質管理・安全管理業務を行う事業所です。製造業については、本記事では実務上わかりやすく製造行為を行う製造所として説明していますが、具体的な該当先は個別の許可内容によって異なる場合があります。府内移転であっても製造業は新規申請が必要な点が製造販売業と大きく異なります。移転を検討している場合は、許可の種類ごとに事前に薬務課へ確認してください。
変更届では対応できない場合
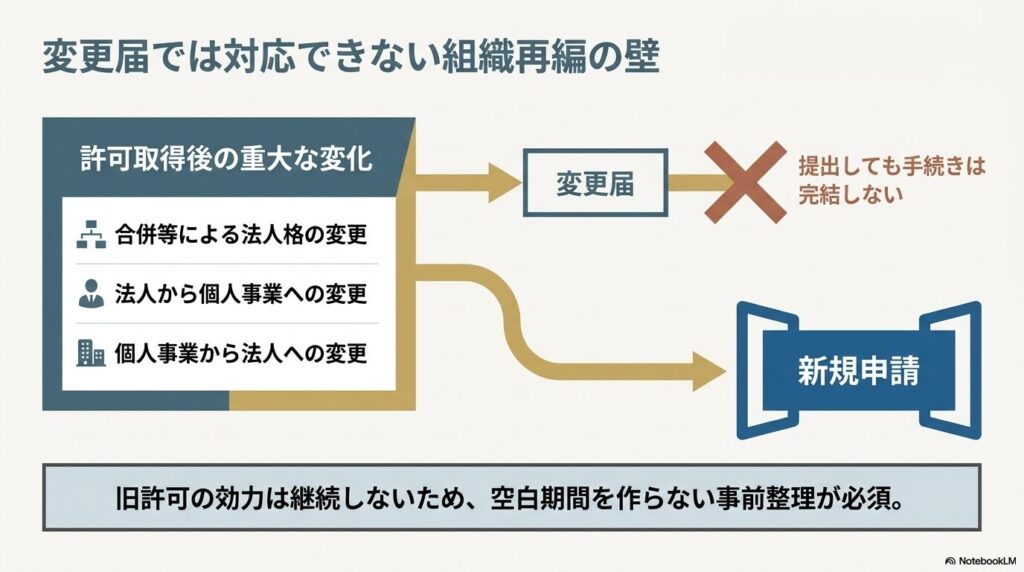
次の場合は変更届ではなく、新たに許可申請が必要です。変更届を提出しても手続きが完結しないため注意が必要です。
- 合併等による法人格の変更(吸収合併・会社分割等)
- 法人から個人事業への変更
- 個人事業から法人への変更
つまり、会社の法人化や組織再編を検討している場合は、化粧品許可の観点から専門家に事前確認することが求められます。法人格が変わった場合、旧許可の効力がそのまま継続するわけではないため、新規申請が完了するまでの期間の対応について事前に整理しておく必要があります。
製品届出の変更手続き
許可の更新・変更届とは別に、製品ごとの届出(化粧品製造販売届出書)にも変更手続きが必要な場合があります。
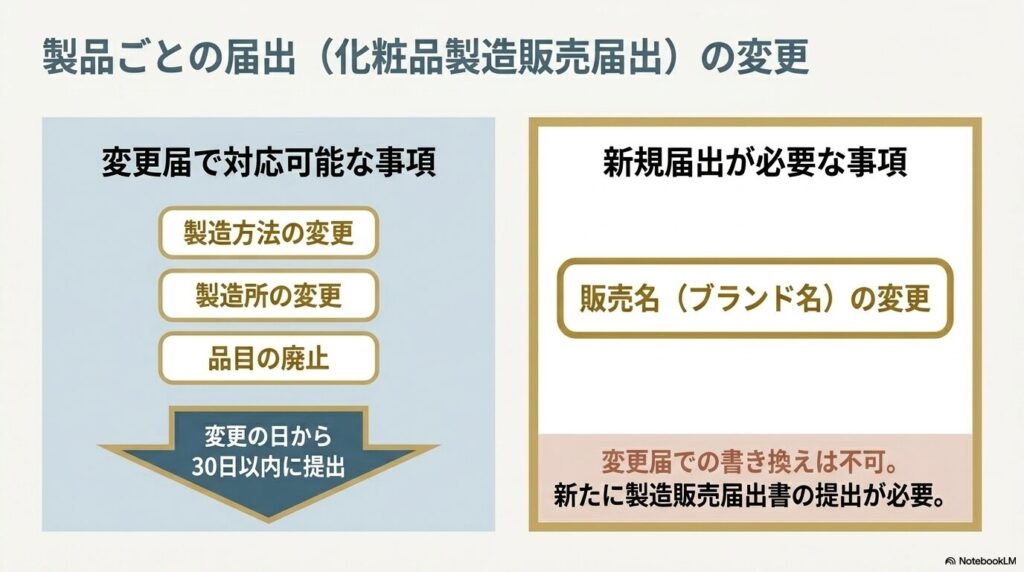
製造方法・製造所・品目の廃止等に変更が生じた場合は、変更の日から30日以内に「化粧品製造販売事項変更届出書」を提出してください(薬機法第14条の9第2項)。
なお、届出済みの販売名を変更する場合は、変更届出書ではなく新たに製造販売届出書を提出する必要があります。変更届で販売名を書き換えることはできないため、品名変更を検討している場合は新規届出として手続きを進めてください。
よくある質問
Q. 責任者が退職しました。何日以内に手続きが必要ですか?
A. 変更の日から30日以内に変更届が必要です(規則第99条)。後任者の選任が決まり次第、速やかに準備を開始してください。製造販売業の場合は総括製造販売責任者、製造業の場合は責任技術者について、後任者が薬機法上の資格要件を満たしているかの確認も必須です。要件を満たす人材がいない場合は、後任選定の段階から専門家に相談することを推奨します。
Q. 更新申請の書類は新規申請と同じですか?
A. 基本的な書類構成は共通していますが、製造販売業では、更新時にGQP・GVP手順書や運用記録の整備状況も確認対象となります。新規申請時の書類一式を控えとして保管しておくと、更新時の準備がスムーズです。許可証の控えと合わせて、申請書類は5年分まとめて保管することを推奨します。
Q. 複数の都道府県で許可を持っている場合、更新はどこへ申請しますか?
A. 各許可を交付した都道府県(主たる機能を有する事務所の所在地を管轄する都道府県)ごとに更新申請が必要です。許可ごとに有効期限が異なる場合があるため、複数の許可を持つ場合は期限一覧を一元管理することを推奨します。
当事務所の強み:化学の専門知識を活かした許可維持サポート
化粧品許可の更新・変更手続きは、新規取得時と同様に専門的な書類準備が必要です。元化学メーカー研究員として化粧品材料の研究開発に携わった経験から、手順書の実態適合性も含めて一貫してサポートします。
- GQP・GVP手順書の現状確認と改善提案(更新審査対応)
- 更新申請書類の作成代行(大阪府対応)
- 責任者変更届・製造販売事項変更届出書の作成
- 法人化・合併時の許可再申請サポート
煩雑な更新・変更手続きを、的確にサポートいたします。行政対応の負担を最小限に抑え、貴社が本来の業務である「化粧品の企画・開発・販売」に専念できるよう伴走いたします。まずはご連絡ください。

