
医薬部外品製造販売業許可とは|化粧品との違いと承認手続きのポイント
※本記事は執筆当時の情報に基づきます。法改正等により現在の内容と異なる場合がありますので、実際の運用にあたっては必ず最新の法令をご確認ください。
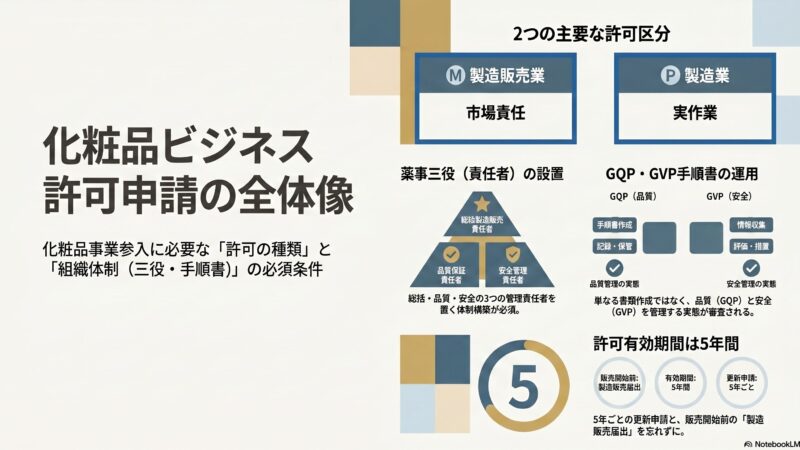
化粧品製造販売業の許可をすでに持っているとしても、「薬用化粧品」を市場に出すには、それだけでは足りません。
薬用化粧品は法律上、化粧品ではなく医薬部外品として扱われます。つまり、医薬部外品製造販売業の許可を別途取得し、さらに製品ごとに製造販売承認を受ける必要があります。
化粧品との制度的な違いを理解することが、薬用化粧品ビジネスへの参入を検討する上で最初のステップです。元化学メーカー研究員として化粧品材料の研究開発に携わった経験から、制度の構造を整理します。
「薬用化粧品」と「医薬部外品」の関係
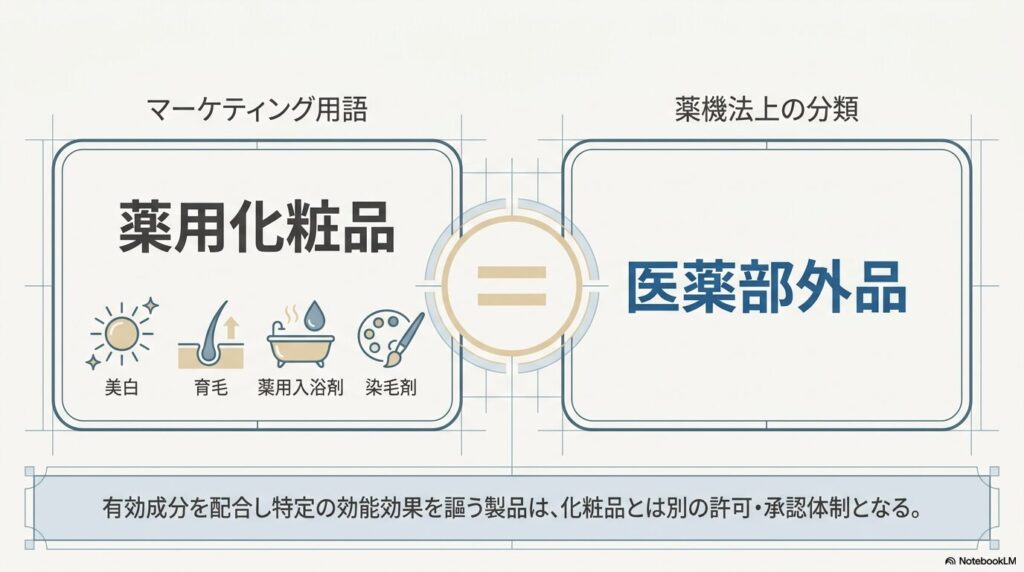
「薬用化粧品」という言葉は、マーケティング用語として広く使われています。しかし薬機法(医薬品医療機器等法)には「薬用化粧品」という区分は存在しません。
薬用化粧品の実態は、薬機法第2条第2項で定義される「医薬部外品」です。具体的には、美白・育毛・薬用入浴剤・染毛剤・パーマネント・ウェーブ用剤などが該当します。有効成分を配合して特定の効能効果を謳う製品は、化粧品ではなく医薬部外品として規制されます。
つまり「薬用〇〇」「医薬部外品」と表示された製品は、化粧品とは別の許可・承認体制のもとで製造・販売されています。
化粧品と医薬部外品の制度的な違い
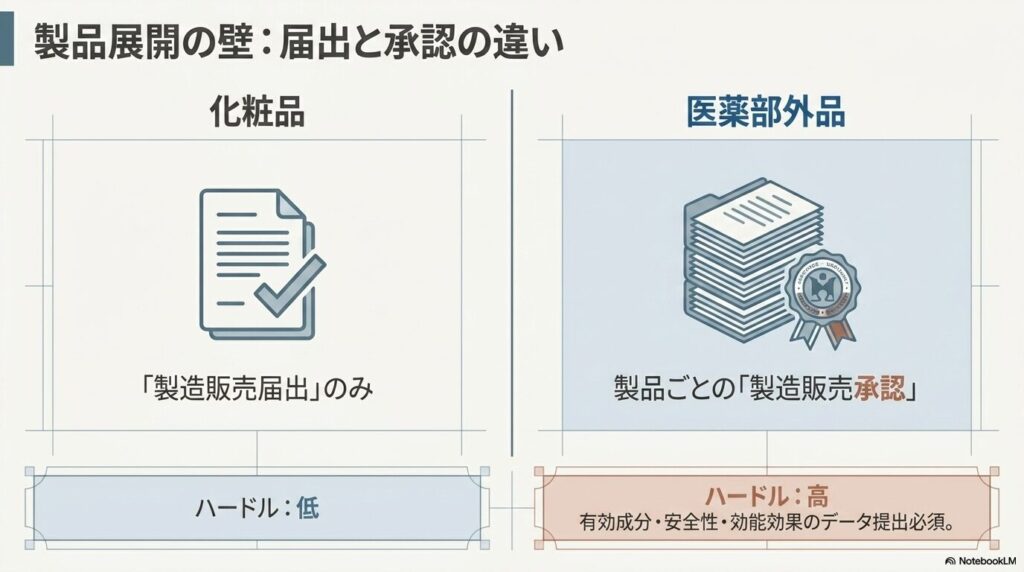
化粧品製造販売業を持つ事業者が医薬部外品に参入するとき、まず確認が必要なのが制度上の差異です。
許可に加えて「承認」が必要
化粧品の製造販売では、製品ごとに「製造販売届出」を提出すれば販売が可能です。一方、医薬部外品は製品ごとに国(厚生労働大臣)の「製造販売承認」を取得することが原則として求められます(薬機法第14条)。
届出と承認では、手続きの難易度と審査期間が大きく異なります。承認審査では有効成分の配合量・安全性・効能効果に関するデータの提出が求められるため、化粧品の届出とは比較になりません。
GMP省令の適用
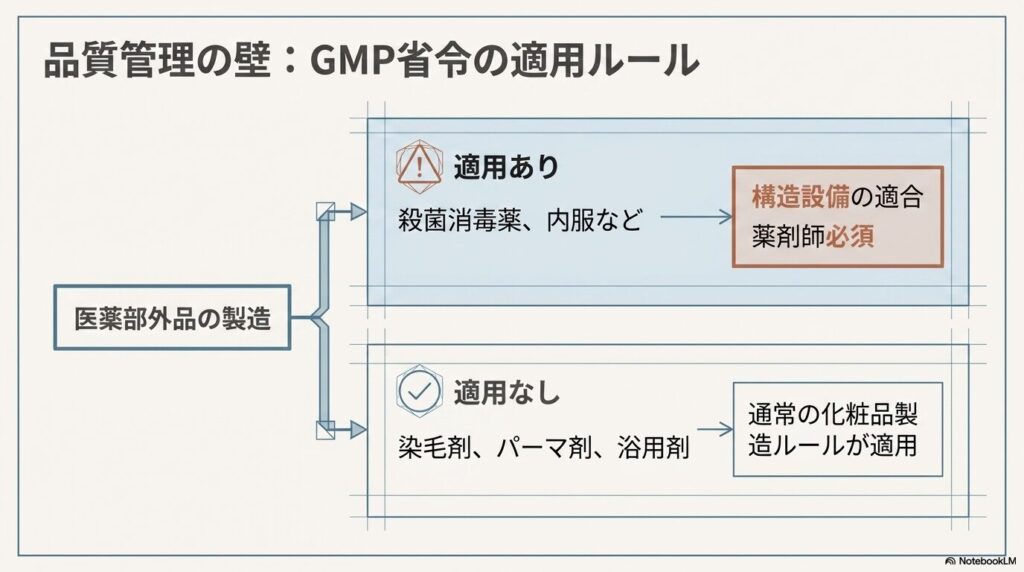
化粧品の製造業にはGMP(Good Manufacturing Practice、製造管理・品質管理基準)の適用義務はありません。しかし、医薬部外品の一部ではGMP省令(平成16年厚生労働省令第179号)が適用されます。
大阪府薬務課の資料によれば、GMP適用となる医薬部外品は、健胃薬・含嗽薬・殺菌消毒薬・滋養強壮剤・ビタミン剤など、内服や特定の外用途に使用される製品です。一方、染毛剤・パーマネント・ウェーブ用剤・浴用剤などはGMP非適用となります。
GMP適用製品を製造する場合、製造所はGMP省令に適合した構造設備を整える必要があります。また、GMP適用製品の製造業では責任技術者に薬剤師が必須となります。
総括製造販売責任者の資格要件の違い
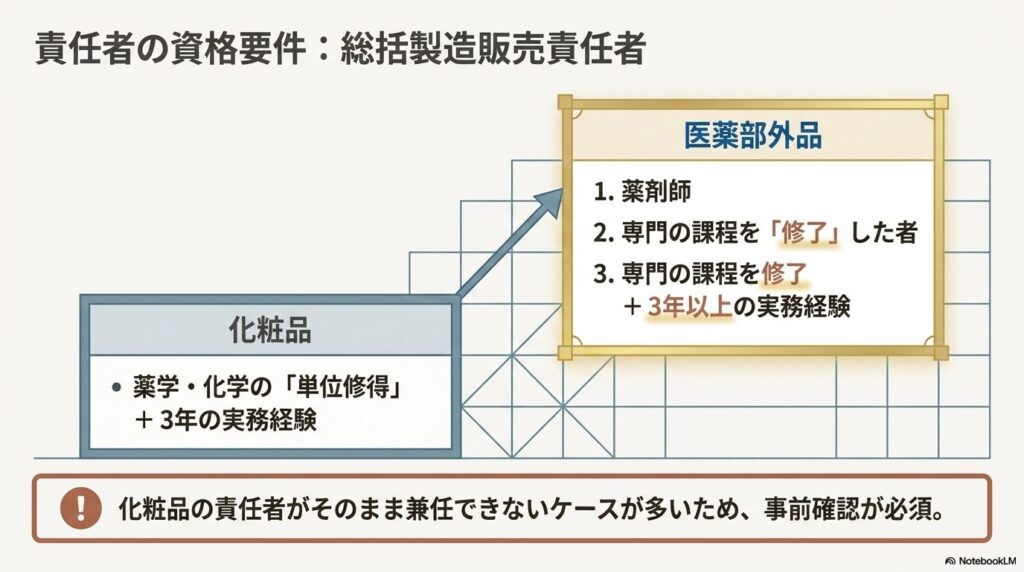
製造販売業の許可において、総括製造販売責任者(総責)の資格要件にも違いがあります。
化粧品の場合、高校や大学で薬学・化学に関する科目を修得すれば、その後3年以上の実務経験でも要件を満たせます。対して医薬部外品は、高校または大学で「薬学または化学に関する専門の課程を修了」した者に要件が絞られています。「科目を修得した」レベルでは医薬部外品の要件を満たさないため、注意が必要です。
具体的には以下のいずれかに該当する者を選任します(薬機法施行規則第85条の2第1項)。
- 薬剤師
- 大学等で薬学または化学に関する専門の課程を修了した者
- 高校等で薬学または化学に関する専門の課程を修了した後、医薬品または医薬部外品の品質管理・製造販売後安全管理業務に3年以上従事した者
- 厚生労働大臣が上記1〜3と同等以上の知識経験を有すると認めた者
化粧品の総責として選任している担当者が、医薬部外品の要件を満たすかどうかを事前に確認することが重要です。
製造販売業許可の取得手順
医薬部外品製造販売業の許可は、都道府県知事(主たる事務所の所在地を管轄する都道府県)へ申請します。標準事務処理期間は60日以内です。
許可要件の確認
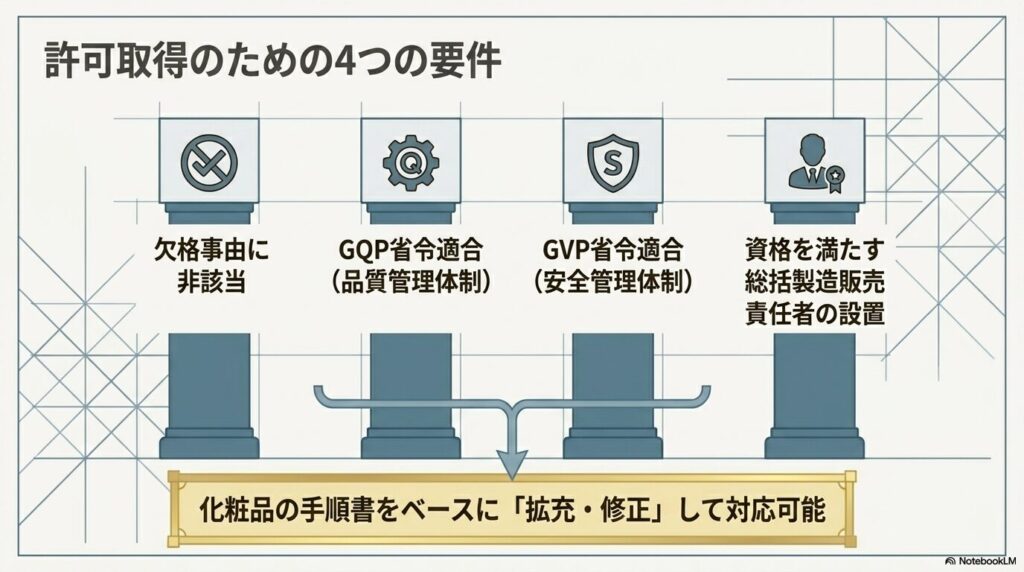
許可を受けるための主な要件は以下のとおりです(薬機法第12条の2)。
- 欠格事由(薬機法第5条第3号イ〜ト)に該当しないこと
- GQP省令(品質管理基準)に適合した管理体制があること
- GVP省令(安全管理基準)に適合した管理体制があること
- 上記の基準を満たす総括製造販売責任者を設置すること
GQP・GVP省令は化粧品の製造販売業でも適用されます。すでに化粧品で手順書を整備している事業者は、医薬部外品向けに内容を拡充・修正する形で対応できます。
GQP・GVP手順書の整備
化粧品と医薬部外品は同じGQP・GVP省令が適用されますが、扱う製品の性格が異なります。医薬部外品は有効成分の管理や承認内容との適合性確認が加わるため、手順書の記載内容もより詳細な対応が求められます。
手順書は許可要件であると同時に、更新審査における確認書類でもあります。自社の実態と合わない手順書は、運用上の矛盾を生みます。形式的な整備にとどまらず、実際の業務フローに即した内容にしておく必要があります。

申請書類の準備と提出
主な提出書類は以下のとおりです(大阪府薬務課、令和5年3月版)。
- 経過表
- 製造販売業許可申請書(医薬品等電子申請ソフトで作成・FDまたはCD提出)
- 登記簿謄本(発行から6ヶ月以内)
- 総括製造販売責任者の資格を証する書類(卒業証明書等)
- 総括製造販売責任者の雇用契約書の写し等
- 組織図・GQP体制図・GVP体制図
- 業者コード登録票(厚生労働省への事前申請が必要)
申請前に、厚生労働省のe-Govで業者コードを登録しておく必要があります。化粧品製造販売業と同一所在地であれば、業者コードの新規登録は不要です。
製品ごとの承認取得
許可の取得後、製品を市場に出すには製品ごとの製造販売承認が必要です。承認申請はPMDA(独立行政法人医薬品医療機器総合機構)経由となる場合もあり、審査に要する期間は製品の種類によって異なります。
製品の承認取得は、許可申請とは別に時間とコストがかかるプロセスです。参入を検討する段階から、対象製品の承認カテゴリや審査期間の目安を把握しておくことが、事業計画の精度を高めます。
よくある質問
Q. 化粧品製造販売業を持っていれば、医薬部外品の手続きはどれくらい省けますか?
A. GQP・GVP省令の対応体制はベースとして活用できます。ただし許可は別途取得が必要であり、製品ごとの製造販売承認も化粧品の届出とは別に行います。「許可を持っているから申請が簡単」ではなく、「体制の一部を転用できる」という理解が正確です。
Q. 薬用シャンプーを自社製造して販売したい。どの許可が必要ですか?
A. 薬用シャンプーは医薬部外品に該当する可能性があります。自社で製造するなら医薬部外品製造業の許可(GMP適用の有無による区分あり)、市場に出荷するなら医薬部外品製造販売業の許可が必要です。さらに製品ごとに製造販売承認を取得する必要があります。製品の成分・効能訴求の内容によって分類が変わるため、計画段階での確認を推奨します。
Q. 医薬部外品の製造販売業許可の有効期間はどれくらいですか?
A. 化粧品と同様に5年間です。継続して事業を行う場合は、期限前に更新申請が必要です。更新時にも実地調査があり、GQP・GVP手順書の運用実績が確認されます。
当事務所の強み
医薬部外品の許可・承認手続きは、化粧品と制度的に共通する部分を持ちながら、より厳格な対応が求められます。
元化学メーカー研究員として化粧品材料の研究開発に携わった経験から、製品の成分・処方レベルで分類の妥当性を確認した上で手続きを進めます。GMP適用の有無の判断や、総括製造販売責任者の資格要件の確認など、制度の解釈が必要な場面で的確な判断を提供します。
- 医薬部外品製造販売業許可申請(新規・更新)
- GQP・GVP手順書の作成・整備(化粧品からの拡充対応を含む)
- 製品分類(化粧品か医薬部外品か)の事前確認サポート
- GMP適用製品に関する構造設備要件の確認
既存の化粧品ライセンスの状況から整理し、必要な追加手続きをまとめてお任せいただけます。

